2 × Taq Platinum PCR Mix
Definición da actividade
1 actividade (U) Taq ADN de platino Polimerase defínese como a cantidade de encima necesaria para incorporar 10 nmol desoxinucleótidos en substancias insolubles en ácidos a 74 ° C dentro de 30 min usando ADN de esperma de salmón activado como molde / cebador.
Control de calidade
A pureza mediante detección SDS-PAGE é superior ao 99%; Non se detecta actividade de nucleasa esóxena; O xene de copia única no xenoma humano podería amplificarse de forma efectiva; Non hai cambios significativos de actividade cando se garda a temperatura ambiente durante unha semana.
Principais parámetros técnicos
Ten actividade de exonucleasa 5′-3 ′ e actividade de exonuclease 3′-5 ′, e a súa fidelidade está xunto á Pfu polimerase. A velocidade de extensión da Taq Platinum Polymerase é máis rápida que a Pfu polimerase e a eficiencia de amplificación é maior. Os produtos de PCR poden ligarse directamente ao extremo contundente ou clonarse cun vector TA. Se hai que mellorar a eficiencia de clonación, recoméndase purificar primeiro e engadir saíntes de 3'-dA antes de clonar no vector TA.
One-tube Taq Platinum MasterMix (certificación nacional de produtos de alta tecnoloxía)
■ O Taq Platinum MasterMix mellorou a especificidade e sensibilidade da reacción PCR e pode amplificar modelos complexos con alto contido en GC, estrutura secundaria e similares. Pódense amplificar ata 2 copias do modelo de destino, asegurando resultados experimentais máis precisos.
■ A única fórmula Taq Platinum MasterMix fai que todo o sistema de reacción sexa moi estable e a actividade non se verá afectada por conxelación-desconxelación repetida nin almacenamento a longo prazo a 4 ° C.
■ A solución mixta de PCR pre-preparada estable e eficiente pode facer a operación rápida e sinxela, reducindo moito a intensidade do traballo e o erro de mostraxe. O mellorador e optimizador de PCR de alto rendemento tamén se inclúen na mestura, o que reduce os requisitos nas condicións de PCR.
■ Este produto ten sistemas que conteñen tintes e sen tintes. Os produtos MasterMix que conteñen colorantes pódense electroforear directamente despois da PCR, sen engadir tampón de carga.
Aplicacións
Pode substituír a Pfu polimerase para amplificar produtos de alta fidelidade de modelos complexos como xenomas e é adecuado para aplicacións como a clonación de xenes de expresión, mutacións específicas do sitio e análise de polimorfismo dun só nucleótido (SNP), etc.
Precaucións no deseño de imprimacións PCR:
A lonxitude da imprimación adoita ser de 20-25 mer. Non obstante, cando se realiza PCR de fragmentos longos, a lonxitude do cebador debe aumentarse a 30-35 mer.
■ Non hai emparellamento complementario entre os dous cebadores, especialmente para as últimas 3 bases no extremo 3 ′.
■ O contido de GC debe ser do 50-60% e evitar GC ou AT rico local. Para que a imprimación e o molde se unan de forma estable, evite a estrutura rica en AT no extremo 3 ′.
■ Evite a imprimación para formar unha estrutura secundaria.
■ Seleccione dous cebadores con temperaturas Tm próximas entre si.
Cálculo do valor Tm dos cebadores para PCR:
■ Cando a imprimación sexa inferior a 20 mer: Tm = 2 ° C × (A + T) + 4 ° C × (G + C).
■ Cando a imprimación é superior a 20 mer: Tm = 81,5 + 0,41 × (GC%) - 600 / L, onde L é a lonxitude da imprimación.
■ Axuste a temperatura de recocido en (Tm-5) ° C.
Entrada de imprimación PCR
A concentración final axeitada de cebadores pode seleccionarse entre 0,1 μM e 1,0 μM. Unha concentración de imprimación moi baixa leva a un baixo rendemento de produtos de amplificación, mentres que unha concentración de imprimación demasiado alta é máis propensa a unha amplificación non específica. Normalmente, cando a cantidade de ADN molde é grande ou complexa utilízase ADN molde (como o ADN do xenoma humano) como molde, a concentración de cebador debe ser menor. Cando a cantidade de ADN molde é pequena ou se usa ADN molde simple (por exemplo, ADN plásmido, etc.) como molde, a concentración de cebador debe ser maior.
Todos os produtos pódense personalizar para ODM / OEM. Para máis detalles,faga clic en Servizo personalizado (ODM / OEM)
 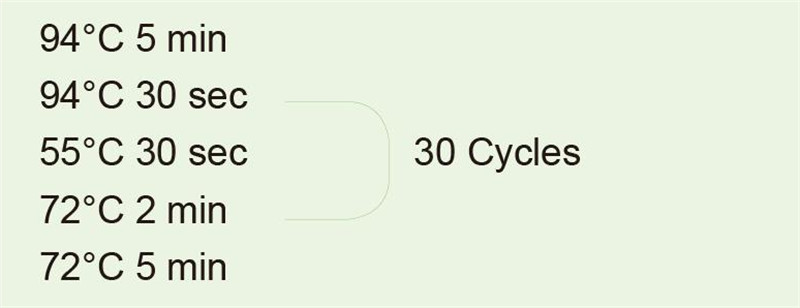 |
Use o ADN xenómico como modelo para amplificar o fragmento de 1 kb. Despois da reacción da PCR, tome 5 μl para a detección de electroforese. |
Modelo A-1
■ O modelo contén impurezas de proteínas ou inhibidores de Taq, etc. —Purificar o modelo de ADN, eliminar as impurezas de proteínas ou extraer o ADN modelo con kits de purificación.
■ A desnaturalización do modelo non está completa - Aumentar adecuadamente a temperatura de desnaturalización e prolongar o tempo de desnaturalización.
■ Degradación do modelo: prepara de novo o modelo.
Imprimación A-2
■ Mala calidade dos cebadores ——Resintetiza o cebador.
■ Degradación de imprimación ——Aliquot os cebadores de alta concentración en pequeno volume para a súa conservación. Evite a conxelación e desconxelación múltiple ou crioconservación a longo prazo de 4 ° C.
■ Deseño inadecuado dos cebadores (por exemplo, a lonxitude do cebador non é suficiente, o dímero formado entre os cebadores, etc.).
A-3 Mg2+concentración
■ Mg2+ a concentración é demasiado baixa —— Aumentar adecuadamente Mg2+ concentración: Optimizar o Mg2+ concentración por unha serie de reaccións de 1 mM a 3 mM cun intervalo de 0,5 mM para determinar o Mg óptimo2+ concentración para cada modelo e cartilla.
A-4 Temperatura de recocido
■ A alta temperatura de recocido afecta á unión da imprimación e do molde. ——Reducir a temperatura de recocido e optimizar o estado cun gradiente de 2 ° C.
A-5 Tempo de ampliación
■ Tempo de extensión curto —— Aumentar o tempo de extensión.
Fenómenos: as mostras negativas tamén mostran as bandas de secuencia obxectivo.
A-1 Contaminación de PCR
■ Contaminación cruzada de produtos de amplificación ou de secuencia diana ——Para non pipetar con precaución a mostra que contén a secuencia diana na mostra negativa nin derramalos fóra do tubo da centrífuga. Os reactivos ou equipos deben ser autoclavados para eliminar os ácidos nucleicos existentes e a existencia de contaminación debe determinarse mediante experimentos de control negativo.
■ Contaminación dos reactivos ——Aliquote os reactivos e almacénelos a baixa temperatura.
A-2 Primer
■ Mg2+ a concentración é demasiado baixa —— Aumentar adecuadamente Mg2+ concentración: Optimizar o Mg2+ concentración por unha serie de reaccións de 1 mM a 3 mM cun intervalo de 0,5 mM para determinar o Mg óptimo2+ concentración para cada modelo e cartilla.
■ Deseño de cebador incorrecto e a secuencia diana ten homoloxía coa secuencia non diana. —— Cebadores de redeseño.
Fenómenos: as bandas de amplificación de PCR son incompatibles co tamaño esperado, grande ou pequeno, ou ás veces prodúcense ambas bandas de amplificación específicas e bandas de amplificación non específicas.
A-1 Imprimación
■ Mala especificidade da imprimación
—— Imprimación de redeseño.
■ A concentración de imprimación é demasiado elevada —— Aumenta adecuadamente a temperatura de desnaturalización e prolonga o tempo de desnaturalización.
A-2 Mg2+ concentración
■ O Mg2+ a concentración é demasiado alta ——Reducir adecuadamente a concentración de Mg2 +: Optimizar o Mg2+ concentración por unha serie de reaccións de 1 mM a 3 mM cun intervalo de 0,5 mM para determinar o Mg óptimo2+ concentración para cada modelo e cartilla.
A-3 Polimerase termoestable
■ Cantidade excesiva de encima ——Reducir a cantidade de enzima adecuadamente a intervalos de 0,5 U.
A-4 Temperatura de recocido
■ A temperatura de recocido é demasiado baixa: aumenta axeitadamente a temperatura de recocido ou adopta o método de recocido en dúas etapas.
A-5 ciclos de PCR
■ Demasiados ciclos de PCR ——Reducir o número de ciclos de PCR.
A-1 Imprimación——Pobre especificidade ——Deseña de novo a imprimación, cambie a posición e a lonxitude da imprimación para mellorar a súa especificidade; ou realizar PCR aniñada.
Modelo ADN A-2
——A plantilla non é pura ——Purifica a plantilla ou extrae ADN con kits de purificación.
A-3 Mg2+ concentración
——Mg2+ a concentración é demasiado alta ——Reducir adecuadamente Mg2+ concentración: Optimizar o Mg2+ concentración por unha serie de reaccións de 1 mM a 3 mM cun intervalo de 0,5 mM para determinar o Mg óptimo2+ concentración para cada modelo e cartilla.
A-4 dNTP
——A concentración de dNTP é demasiado alta ——Reduce a concentración de dNTP adecuadamente
A-5 Temperatura de recocido
——Temperatura de recocido demasiado baixa—— Aumentar adecuadamente a temperatura de recocido
Ciclos A-6
——Moitos ciclos ——Optimiza o número de ciclos

O primeiro paso é escoller a polimerase axeitada. A polimerase Taq regular non pode revisarse debido á falta de actividade de exonucleasa 3'-5 ', e o desaxuste reducirá moito a eficiencia de extensión dos fragmentos. Polo tanto, a polimerase Taq regular non pode amplificar con eficacia fragmentos diana maiores a 5 kb. A taq polimerase con modificación especial ou outra polimerase de alta fidelidade debe seleccionarse para mellorar a eficiencia da extensión e satisfacer as necesidades de amplificación de fragmentos longos. Ademais, a amplificación de fragmentos longos tamén require un axuste correspondente do deseño da imprimación, o tempo de desnaturalización, o tempo de extensión, o pH do tampón, etc. Normalmente, os imprimadores con 18-24 pb poden levar a un mellor rendemento. Para evitar danos na plantilla, o tempo de desnaturalización a 94 ° C debería reducirse a 30 segundos ou menos por ciclo e o tempo para subir a temperatura a 94 ° C antes da amplificación debería ser inferior a 1 min. Ademais, establecer a temperatura de extensión a uns 68 ° C e deseñar o tempo de extensión segundo a velocidade de 1 kb / min pode garantir unha amplificación efectiva de fragmentos longos.
A taxa de erro da amplificación por PCR pode reducirse empregando varias ADN polimerasas con alta fidelidade. Entre todas as ADN polimerases de Taq atopadas ata o momento, o encima Pfu ten a taxa de erro máis baixa e a fidelidade máis alta (ver táboa adxunta). Ademais da selección de encimas, os investigadores poden reducir aínda máis a taxa de mutación da PCR optimizando as condicións de reacción, incluíndo a composición do tampón, a concentración de polimerase termoestable e o número de ciclos de PCR.
Categorías de produtos
POR QUE NOS ELIXIR
Dende a súa creación, a nosa fábrica está a desenvolver produtos de primeira clase mundial co cumprimento do principio
de calidade primeiro. Os nosos produtos gañaron unha excelente reputación na industria e confianza valiosa entre clientes novos e antigos ..








